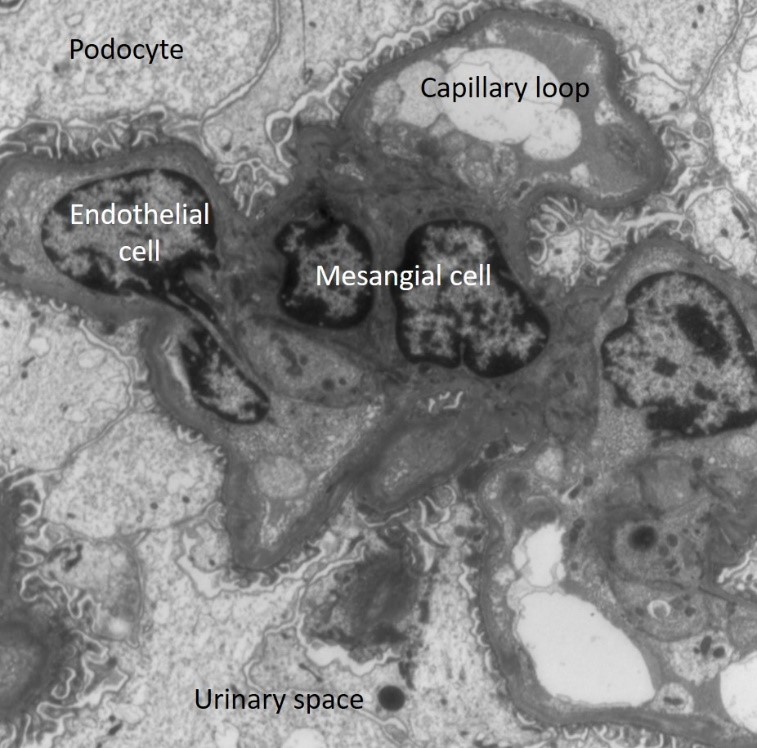
정상 사구체
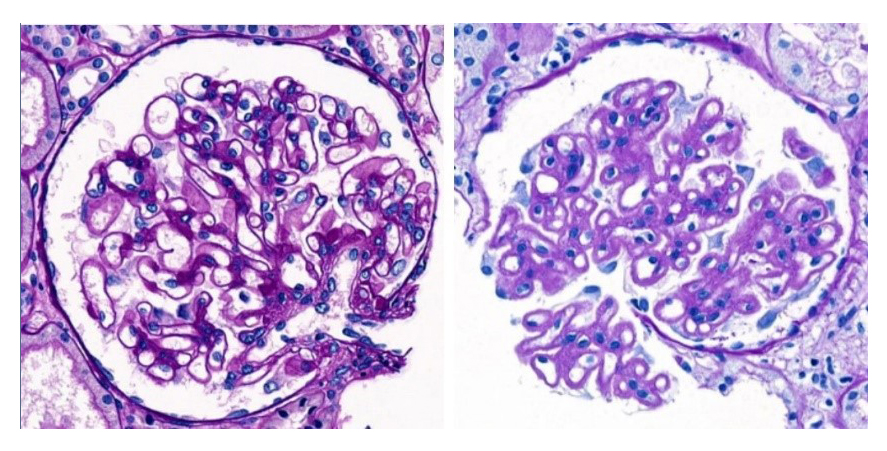
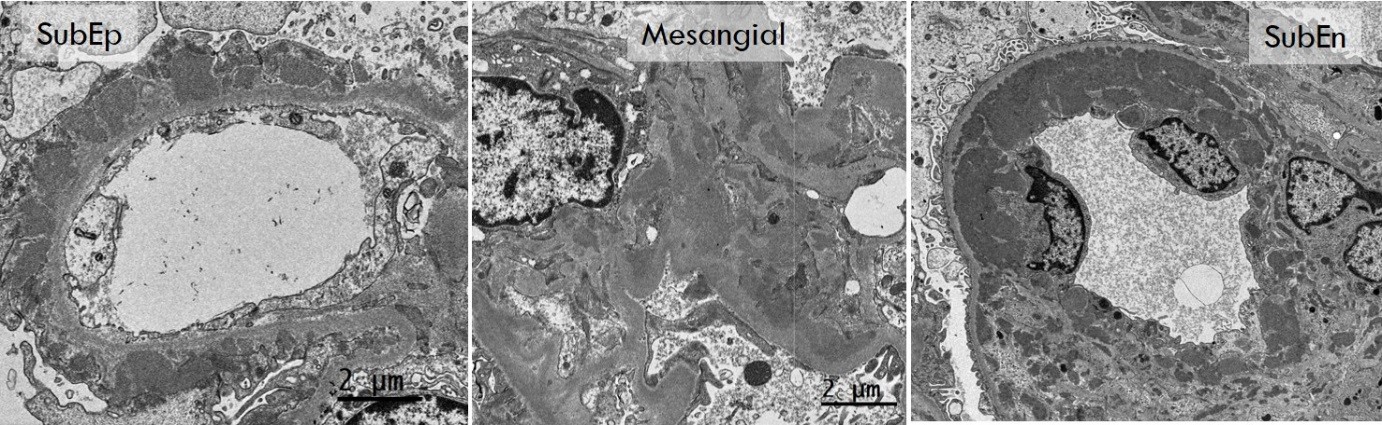
<그림 1-3. 정상 두께의 GBM(좌)과 두꺼워진 GBM(우)>
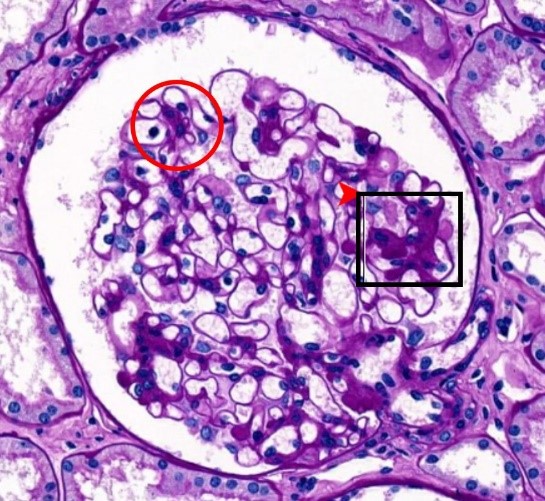
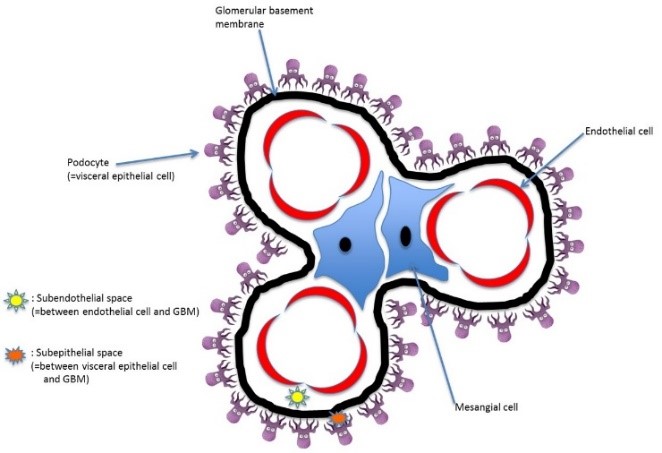
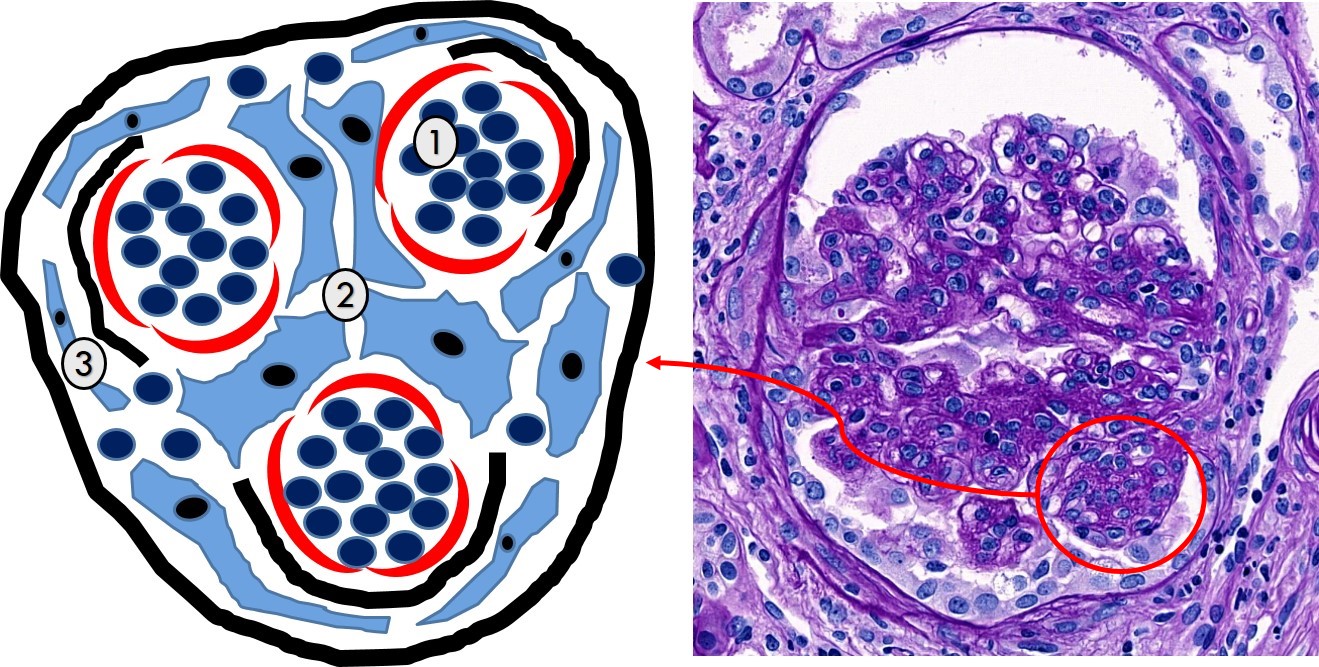
- <그림 1-4.>
- Mesangial cellularity는
단위 mesangium당 세포의 수로
판정한다.
- 붉은 동그라미는 정상 mesangial
cellularity.
- 검은 네모는 mesangial
hypercellularity.
Diffuse vs. Focal / Global vs. Segmental
Sclerosis
Mesangial hypercellularity
Endocapillary hypercellularity
Extracapillary hypercellularity (=crescent)
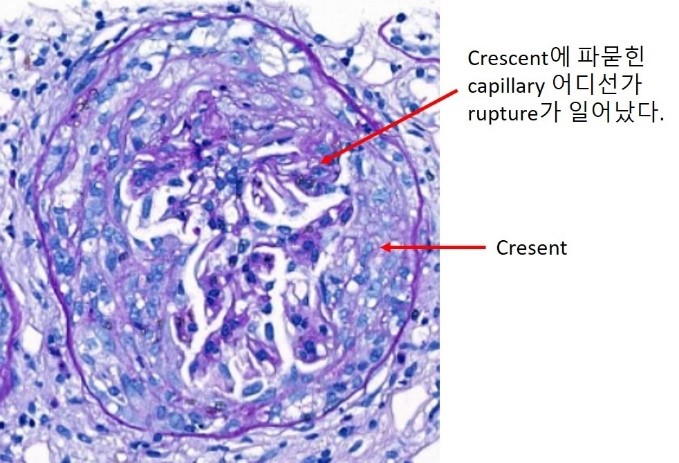
<그림 1-5.>
Parietal epithelial cell이 증식하여 crescent (이 사구체에서는 초승달 단계를 지나 원형을
이룸)를 형성.
Fibrinoid necrosis
Double contour, spike
확대하시려면 이미지를 클릭해주세요.
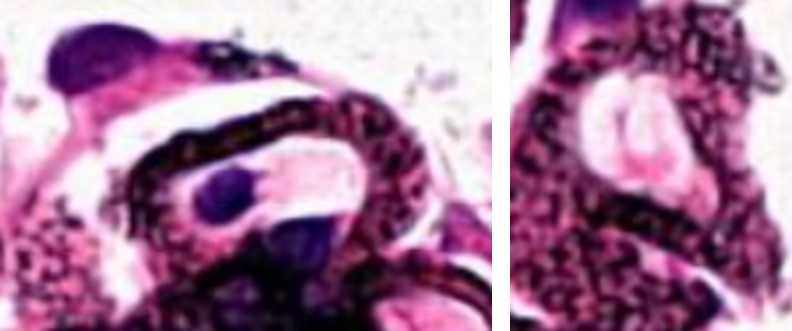
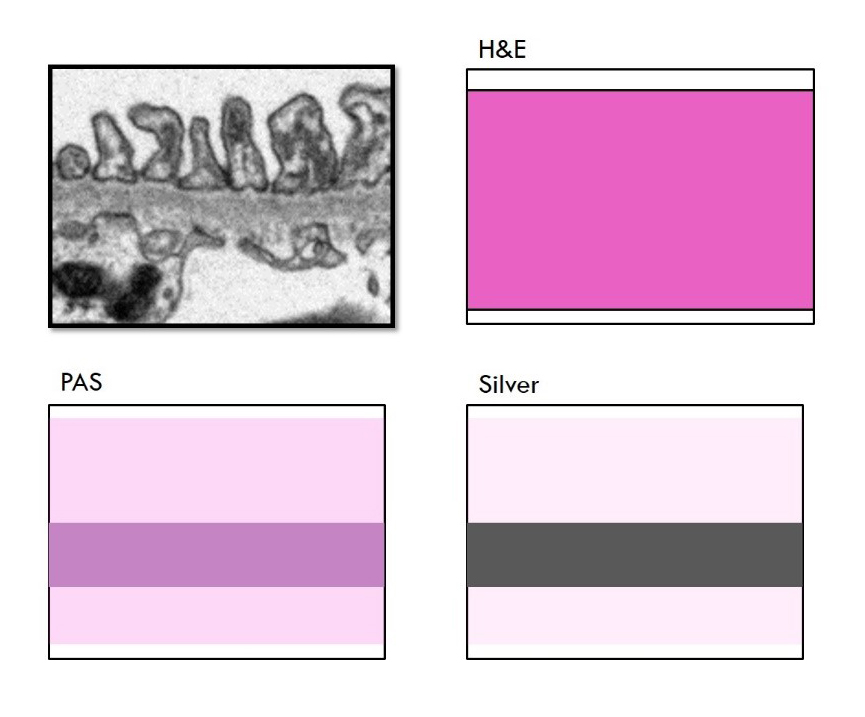
<그림 1-6. Silver 염색에서 보이는 spike. 오른쪽 사진은 spike가 완전하게 생기기 전 immune complex로
인해 울퉁불퉁해진 GBM을 en face로 보게 될 때의 장면이다.>
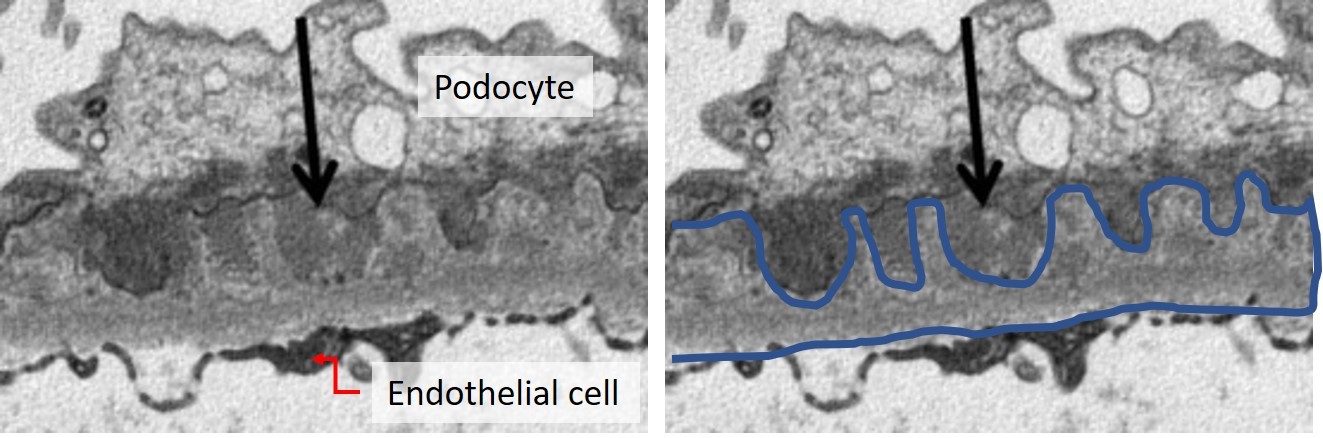
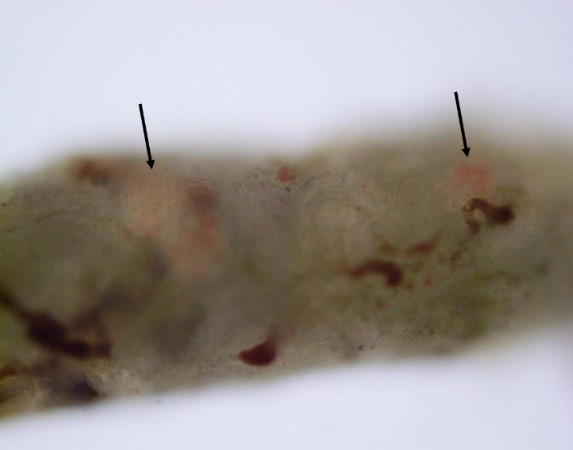
<그림 1-7. Subepithelial immune complex deposit과 이로 인한 GBM의 spike 형성. GBM의
바깥쪽에 immune complex (검은 화살표)가 침착하면 사이사이로 GBM이 자라들어간다. Silver 염색은 GBM 자체를 검은색으로 염색하므로 이 부분이
spike로 보인다. >